



Fakultät für Chemie
Anorganische Chemie III
wer will kann sich wenn er mit der linken
Maustaste hier klickt auch
meine ganze Arbeit als pdf-Datei runterladen, aber es sei
gewarnt, ist über 3 MB groß, runterladen könnte also etwas
dauern, ansonsten hier eine kleine Einleitung.
Die organische
Chemie der Hauptgruppenelemente hat in den letzten drei
Jahrzehnten eine sprunghafte Entwicklung erfahren. Dem Silicium
wurde dabei als Nachbarelement des Kohlenstoffs eine besondere
Beachtung geschenkt. Lange Zeit beschränkte sich die Chemie des
Siliciums auf die Oxidationsstufen 0 und +IV; die Oxidationsstufe
+II spielte lediglich eine untergeordnete Rolle. Die den Carbenen
analogen divalenten Siliciumspezies werden als Silylene
bezeichnet. Si(II)-Verbindungen sind hochreaktive Spezies, die
oftmals nur durch Abfangreaktionen nachgewiesen werden können.
Silylene sind die entscheidenden Zwischenstufen in vielen
thermischen und photochemischen Reaktionen von
Organosilicium-Verbindungen. Schon seit den dreißiger Jahren
sind anorganische Silylene (Hal2Si, O=Si, oder S=Si)
bekannt. Diese lassen sich aber aufgrund ihrer extremen
Instabilität nur mit beträchtlichem experimentellen Aufwand
untersuchen. Der Prototyp organischer Silylene ist das
Dimethylsilylen. H. Gilman et al. konnten 1964 erstmals
Dimethylsilylen als reaktives Intermediat nachweisen. Im Jahre
1979 gelang es R. West et al., diese Spezies mit Hilfe der
Tieftemperatur-Matrix-Isolationstechnik spektroskopisch (UV/VIS-
und IR- Spektroskopie) zu charakterisieren. Versuche, Silylene
durch sterisch anspruchsvolle Liganden zu stabilisieren, waren
lange Zeit nur von mässigem Erfolg. Ein anschauliches Beispiel
hierfür ist das (2,4,6-Tri-iso-propyl)phenyl-
(1,2,3-tris-tert-butylcyclopropenyl)silylen, welches zwar in
Lösung nachgewiesen, aber nicht isoliert werden konnte.
Inzwischen gelang die Synthese einiger stabiler Silylene. Im
Jahre 1990 konnten H.H. Karsch et al. durch Reduktion von
Hexachlordisilan in Gegenwart von Lithiumdiphosphinomethanid eine
kristallisierbare monomere Si(II)-Verbindung darstellen. Die
Stabilisierung dieser vierfach koordinierten Si(II)-Verbindung
erfolgt durch intramolekulare Koordination der
Phosphinomethanid-Liganden an das Siliciumatom und des damit
verbundenen Chelateffektes. Erst 1994 wurde von M. Denk und R.
West eine dem "Arduengo-Carben" analoge, zweifach
koordinierte Si(II)-Verbindung dargestellt und in Substanz
isoliert. Dieses Silylen unterliegt einer Stabilisierung durch
elektronische Effekte. Kurze Zeit später wurden von M.F. Lappert
et al. ähnliche Silylene dargestellt. Erst kürzlich
veröffentlichten J. Heinicke et al. das erste stabile
unsymmetrische Silylen.
In diesem Arbeitskreis gelang es 1986 erstmals, durch die
Verwendung des Pentamethylcyclopentadienyl-Liganden eine bei
Raumtemperatur stabile Si(II)-Verbindung darzustellen, das
Decamthylsilicocen.
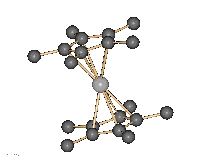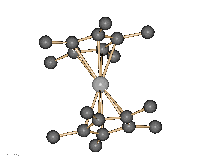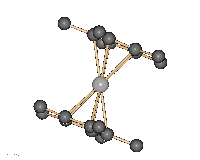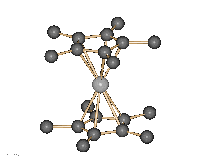
Diese Verbindung
zeichnet sich duch einen sandwichartigen Aufbau aus.
Decamethylsilicocen ist demnach das erste bei Raumtemperatur
beständige Silylen und der erste p-Komplex
des Siliciums. Die Reaktionen mit dieser einzigartigen Verbindung
führt zu interessanten und oftmals nicht erwarteten Ergebnissen.
Die Chemie von Decamethylsilicocen ist der Mittelpunkt meiner
Arbeit. Dabei stehen Untersuchungen zur Reaktivität des
Decamethylsilicocens in Umsetzungen mit
Übergangsmetallverbindungen im Vordergrund. Ausserdem soll nach
potentiellen neuen Ausgangsverbindungen zu Synthese gesucht
werden.